Accueil > Équipes scientifiques > Structure et dynamique des systèmes complexes isolés photoexcités (SYSIPHE) > Molécules Agrégats Neutres Ionisés ou Protonés (MANIP) > Fragmentation de peptides protonées
Fragmentation de peptides protonées
Mécanismes de photo-fragmentation UV
par - 20 mars 2010 (modifié le 19 février 2020)
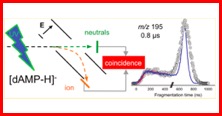
L’expérience « Arc-en-Ciel » installée au Centre National de Cinétique Rapide - ELYSE (Laboratoire de Chimie Physique, Bâtiment 349) est l’élément clef de ces études. Cette expérience, unique au monde, permet de suivre complètement la dynamique de fragmentation en détectant en coïncidence les fragments ioniques et neutre(s) issus de la dissociation d’une même molécule parente, avec des détecteurs sensibles en temps et en position. La spécificité de cette technique permet, par l’analyse des corrélations vectorielles, d’étudier le nombre d’étapes de fragmentation et dans quel l’ordre elles se produisent. L’autre aspect unique de cette expérience est la possibilité de suivre la dynamique de fragmentation de la nanoseconde à la milliseconde.
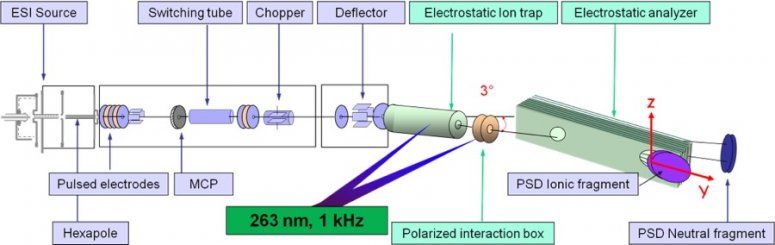
Interactions ion-dipîole induit
Lors de la fragmentation d’un ion monochargé, la détection en coïncidence avec le dispositif Arc-en-Ciel permet de remonter au type de mécanisme de fragmentation (direct ou séquentiel) et d’accéder au temps de fragmentation. Nous avons exploité ce dispositif original et unique à la photodissociation UV pour étudier l’évolution du temps de fragmentation associé à la rupture directe de la liaison Cα-Cβ dans un ensemble de dipeptides protonés contenant d’une part le tryptophane et d’autre part la tyrosine comme chromophore UV. Bien que les mécanismes proposés pour ces ruptures photospécifiques dans les petits peptides soient similaires avec le tryptophane ou la tyrosine comme chromophore UV, la rupture Cα-Cβ avec le tryptophane donne lieu à la perte du résidu ionique (m/z 130) alors que la même rupture avec la tyrosine conduit à la perte du résidu neutre (masse 107). Cette différence est due aux potentiel d’ionisation des deux fragments. Cependant, le temps de fragmentation mesuré pour la rupture de la liaison Cα-Cβ est toujours très court, proche de la limite expérimentale de 20 ns, dans le cas de la tyrosine et augmente avec la taille du système pour les dipeptides contenant le tryptophane (figure ci-dessous).
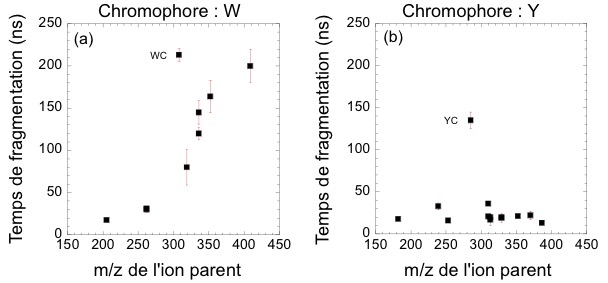
Ces évolutions de temps de fragmentation sont compatibles avec un modèle d’interaction entre une charge ponctuelle (fragment ionique) et un dipôle induit (fragment neutre). Après rupture de la liaison Cα-Cβ, le fragment ionique et le fragment neutre sont faiblement liés par une interaction de type charge - dipôle induit et forment un complexe. Pour l’ensemble des systèmes contenant le tryptophane, l’ion fragment est identique. Le potentiel d’interaction directement proportionnel à la polarisabilité du fragment neutre augmentera avec la masse du fragment neutre. Cette étude systématique sur un ensemble de dipeptides photoexcités à 263 nm démontre que le temps de fragmentation mesurée est caractéristique de l’interaction des fragments dans le complexe formé après la rupture de la liaison Cα-Cβ.
Rupture d’un pont disulfure
L’étude de systèmes complexes contenant un pont disulfure est une nouvelle problématique de recherche du groupe. Le premier volet de cette étude concerne la cystine protonée, qui représente le système modèle le plus simple constitué de deux acides aminés liés par un pont disulfure. L’étude de la dynamique de photodissociation à 263 nm (4,7 eV) a permis d’identifier deux types de ruptures de liaisons (figure ci-dessous), l’un correspondant à la rupture du pont disulfure (S-S) et l’autre à la rupture de la liaison (C-S) adjacente. Nous avons montré que la rupture (S-S) conduit à la formation de trois fragments ioniques de m/z différents associés à des mécanismes de fragmentation spécifiques. Les temps de fragmentation mesurés sont tous inférieurs à 20 ns.
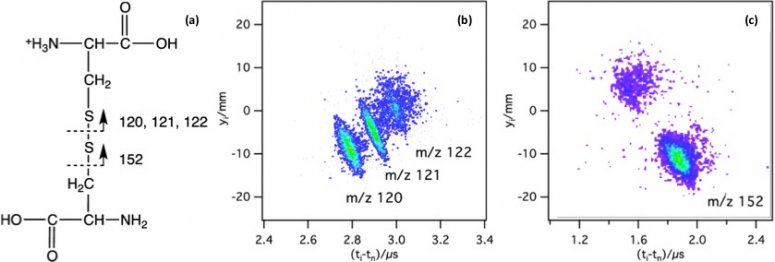
Cette étude nous a permis de mettre en évidence et de caractériser les différentes voies de fragmentations accessibles quand l’excitation UV est localisée au niveau du pont disulfure. La deuxième étape a porté sur la dissociation de systèmes modèles possédant un pont disulfure directement liée à un chromophore aromatique. Nous avons ainsi montré que toutes les fragmentations sont induites par le transfert de proton du groupe amine à l’exception de la rupture homolytique du pont disulfure comme dans la cystine protonée. Ceci a été démontré lors de la protection du groupe amine par l’éther 18-couronne-6.
Transfert d’électron et transfert de proton
L’excitation à 263 nm de dipeptides contenant soit la tyrosine soit le tryptophane fait apparaitre des voies de dissociation spécifiques que sont la rupture Cα-Cβ et la rupture z. Ces ruptures sont interprétées à l’aide du modèle suivant (figure ci-dessous) : le couplage de l’état ππ* localement excité avec (a) un état ππ*CO localisé sur le groupement carbonyle situé en C terminal suivi d’un transfert de proton donne lieu à la rupture de la liaison Cα-Cβ et (b) un état ππ*CO localisé sur le groupement carbonyle situé en N terminal suivi d’un transfert de proton conduit à la rupture z.
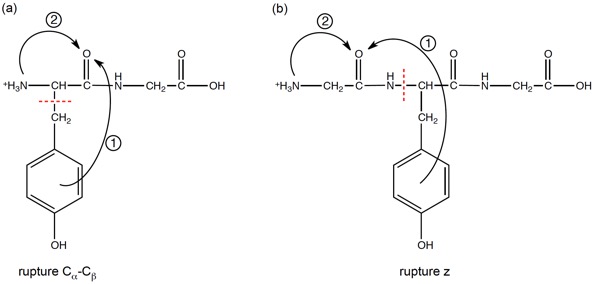
Pour tester ce modèle nous avons étudié ces voies de dissociation pour différentes séquences de petits peptides en faisant, soit varier la position du proton par rapport au chromophore soit en le bloquant. L’étude de la photofragmentation des peptides contenant la Tyrosine YG, YA, AY, GY et GYG a montré que ces voies de dissociation sont toutes observées lorsque l’état à transfert de charge est accessible énergétiquement avec un photon à 263 nm.
Photofragmentation du Tryptophane protonée et de petits peptides protonés à 263 nm
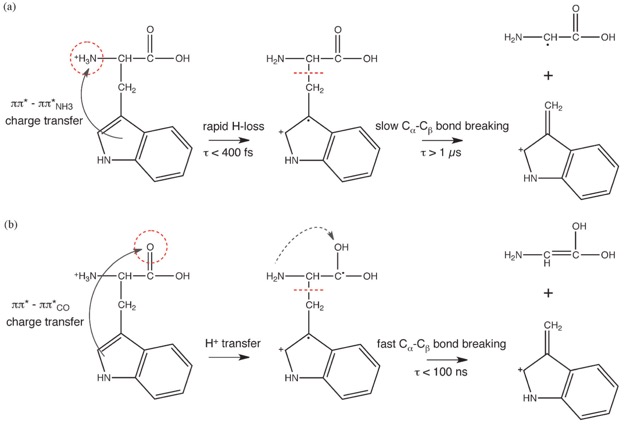
Ainsi dans le cas du tryptophane protoné, on a montré qu’un fragment ionique qui, d’après sa masse, était associé à une fragmentation en trois étapes provient d’une dissociation binaire rapide en moins de 10 ns. Nous avons aussi pu mettre en évidence que le mécanisme de perte du résidu indolique est un processus de fragmentation direct à l’état excité. Dans le cas du tryptophane protoné ces expériences de coïncidence associées aux mesures femtoseconde et à des calculs ab-initio, nous ont permis de donner une vision complète de la dynamique de fragmentation de ce système. Sur des plus gros systèmes (exemple : Glycine-Tryptophane-Glycine) nous avons pu mettre en évidence des fragmentions non ergodiques et proposer des mécanismes qui relient la structure secondaire du peptide avec les voies de fragmentations.
Références :
Dans la même rubrique :


