Accueil > Équipes scientifiques > Structure et dynamique des systèmes complexes isolés photoexcités (SYSIPHE) > Molécules Agrégats Neutres Ionisés ou Protonés (MANIP) > Peptides protonés
Peptides protonés
Dynamique femtoseconde
par - 20 mars 2010 (modifié le 19 février 2020)
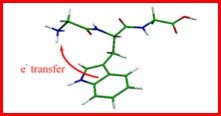
Au cours de ces dernières années, la collaboration menée au laboratoire ELYSE avec le LPL nous a conduit à la découverte d’un état dissociatif similaire à celui qui régit la durée de vie des molécules aromatiques neutres, état qui joue un rôle prépondérant dans la dynamique des états excité des acides aminés et des peptides protonés.
Des expériences pompe/sonde femtoseconde menées sur des acides aminés protonés (tryptophane, tyrosine…) nous ont permis de mettre en évidence la présence d’un état localisé sur le groupement amine terminal. Cet état qui est fortement couplé à l’état initialement excité induit toute une série de processus :
a) une durée de vie de l’état excité très courte (400 fs pour le tryptophane et 20 ps pour la tyrosine)
b) la perte d’un atome d’hydrogène qui mène à la formation d’un ion radicalaire à couche ouverte et qui a donc une réactivité très grande et subit des fragmentations secondaires.
c) la courbe de potentiel de l’état croise celle de l’état fondamental, ce qui mène à une intersection conique où l’hydrogène a une certaine probabilité de se recombiner, ce qui correspond à un processus de conversion interne où l’énergie du photon est transformé en énergie de vibration dans l’état fondamental de l’ion protoné. Cette énergie mène alors à la fragmentation de l’ion suivant des canaux qui ne sont pas les mêmes que ceux observé lors de la perte d’hydrogène.
Ces observations nous ont conduit à examiner si la présence de ces états dissociatifs pouvait induire des ruptures sélectives dans de petits peptides.
Nos observations et nos calculs de chimie quantique semblent montrer qu’il est sans doute possible de fragmenter de manière plus fine et moins brutale avec des photons.
Profitant de la présence de ces états dissociatifs, on doit pouvoir mettre de l’énergie sélectivement dans certaines régions d’un peptide avec des photons. La perte d’un hydrogène ou sa recombinaison immédiate conduira à un apport d’énergie localisé qui induira sans doute des ruptures sélectives dans le peptide.
Cette prédiction optimiste s’est confirmée avec de très récentes expériences menées sur des systèmes plus gros, des dipeptides, tri et pentapeptides. Nous venons d’observer qu’en effet l’excitation optique de dipeptides conduit à des fragmentations qui ne sont pas celles observées lors des fragmentations induites par collision. Ces expériences montrent :
D’une part que les fragmentations dépendent de la géométrie initiale, ce qui implique que les fragmentations sont très loin d’être statistiques même dans une molécule de cette taille.
D’autre part que l’on peut exercer un contrôle des voies de fragmentations en utilisant des impulsions ultra courtes.
les auteurs
H. Kang, C. Jouvet, C. Dedonder, S. Martrenchard, G. Grégoire, C. Desfrançois, J-P. Schermann, M. Barat and J.A. Fayeton
Les publications
Photo-Induced Dissociation of protonated tryptophan TrpH+:a direct dissociation channel via the excited state of the indole chromophore, , H. Kang, C. Dedonder-Lardeux, C. Jouvet, S. Martrenchard, G. Grégoire, C. Desfrançois, J-P. Schermann, M. Barat and J.A. Fayeton
Phys. Chem. Chem. Phys. 6 (2004) 2628.
Photo-induced processes in protonated tryptamine, C. Jouvet, H. Kang, C. Dedonder-Lardeux, S. Martrenchard, C. Charrière, G. Grégoire, C. Desfrançois, J-P. Schermann, M. Barat and J.A. Fayeton, J.Chem. Phys. 122 (8) : Art. No. 084307 FEB 22 2005.
Ultrafast deactivation mechanisms of UV excited states in protonated aromatic amino acids, H. Kang, C. Jouvet, C. Dedonder-Lardeux, S. Martrenchard, G. Grégoire, C. Desfrançois, J-P. Schermann, M. Barat and J.A. Fayeton. Phys. Chem. Chem. Phys 7 (2) : 394-398 2005
Control of bond-cleaving reactions of free protonated tryptophan ion by femtosecond laser pulses, H. Kang, C. Dedonder-Lardeux, C. Jouvet, G. Grégoire, C. Desfrançois, J.-P. Schermann, M. Barat and J. A. Fayeton.J. Phys. Chem. A 109 (11) : 2417-2420 (2005)
Statistical vs non statistical deactivation pathways in the UV photo-fragmentation of protonated tryptophan-leucine dipeptide. Grégoire, H. Kang, C. Dedonder-Lardeux, C. Jouvet, C. Desfrançois, D. Onidas, V. Lepere and J.A. Fayeton. PCCP 8 (1) : 122-128 2006
UV photoinduced dynamics in protonated aromatic amino acid.
Gregoire, G. ; Lucas, B. ; Barat, M. ; Fayeton, J. A. ; Dedonder-Lardeux, C. ; Jouvet, C., European Physical Journal D 2009, 51, (1), 109-116.
Voir en ligne : Photo-Induced Dissociation of protonated tryptophan TrpH+
|
poster_experiences_femtosecondes - 1.9 Mio |


